W jaki sposób nauczyć się rozwiązywać zadania z fizyki? - Część 26
- Szczegóły
- Kategoria: Zadania z fizyki
- Opublikowano: czwartek, 18, maj 2017 11:42
- Autor : Janusz Szcząchor
- O mnie:
- Nauczyciel w Centrum Nauki i Biznesu ŻAK w Łodzi oddział w Grudziądzu
zadanie nr 2.21, Henryk Kaczorek, Zbigniew Słówko - "Zbiór zadań z fizyki", WSiP, Warszawa 1981
W idealnej maszynie chłodniczej wykorzystującej odwrotny cykl Carnota, następuje przekazywanie ciepła od ciała o temperaturze T2 = 253 K (-20°C) do wody o temperaturze T1 = 283 K (10°C). Znajdź ciepło Q2 pobrane od chłodzonego ciała w czasie, gdy praca sił zewnętrznych nad chłodziarką wynosiła W = 118,6 kJ.
zadanie nr 2.19, Henryk Kaczorek, Zbigniew Słówko - "Zbiór zadań z fizyki", WSiP, Warszawa 1981
Oblicz objętość końcową V2 podczas adiabatycznego rozprężania V1 = 3 dm3 gazu w silniku Carnota, którego sprawność wynosi η = 25 %. Stosunek Cp/CV = κ = 2.
Rozwiązanie zadania 2.21
Rozwiązanie tego zadania stanie się proste, jeżeli zauważymy, że sprawność silnika cieplnego w cyklu Carnota, w którym substancją roboczą jest gaz doskonały jest dana nie tylko poprzez ogólny wzór wyrażający ją poprzez ciepło, ale także poprzez temperatury i nie ma tu znaczenia czy silnik Carnota pracuje jako silnik cieplny, czy też jako maszyna chłodząca.
Zatem sprawność maszyny chłodzącej możemy wyrazić jako
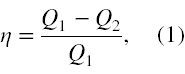
gdzie Q2 to ciepło usuwane ze zbiornika o niższej temperaturze T2, a Q1 to ciepło dostarczane do zbiornika o wyższej temperaturze T1. Biorąc pod uwagę, że praca sił zewnętrznych nad chłodziarką jest dana jako W = Q1 - Q2 możemy wzór (1) wyrażając przez dane zadania zapisać jako
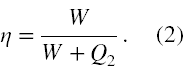
Z drugiej strony wyrażając sprawność poprzez temperatury zbiorników z ciepłem możemy otrzymać następującą równość
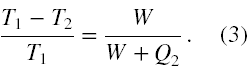
Wykorzystując własność proporcji, na podstawie wzoru (3) możemy zapisać, że ( T1 - T2 )( W + Q2 ) = T1· W. Po wykonaniu odpowiednich przekształceń algebraicznych otrzymujemy z tej równości rozwiązanie w postaci wzoru (4)
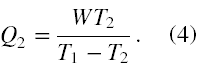
Rozwiązanie zadania 2.19
Gaz roboczy w silniku Carnota podczas rozprężania adiabatycznego przechodzi od stanu opisanego parametrami p1, V1, T1 do stanu opisanego parametrami p2, V2, T2 nie przestając być gazem doskonałym. A zatem ma do niego zastosowanie poniższa konsekwencja równania Clapeyrona
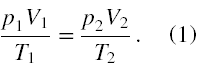
Zauważmy, że parametry ciśnienie, objętość i temperatura tworzą w tym równaniu trzy pary, a raczej trzy ilorazy. Iloraz temperatur da się określić poprzez podaną w zadaniu sprawność, czyli
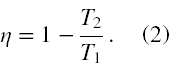
Z kolei iloraz ciśnień da się określić na podstawie konsekwencji wynikającej ze związku ciśnienia i objętości w przemianie adiabatycznej pVκ = const., czyli
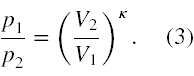
Zatem podstawiając wnioski ze wzorów (2) i (3) do (1) otrzymujemy związek między V1 i V2 w następującej postaci
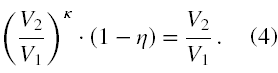
Wzór (4) dzielimy stronami przez V2 i (1 - η), mnożymy stronami przez (V1)κ. Otrzymujemy
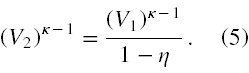
Pozostaje wykonać stronami pierwiastkowanie rzędu κ-1 i ostateczny wynik to